学术动态
肖意传/郑明月研究组合作揭示CD4 T细胞中新的DNA感知通路及其介导衰老相关自身免疫病的调控机制
作者:肖意传 来源自:中国免疫学会 点击数:37071 发布时间:2021-04-28
2021年4月13日,国际学术期刊Immunity发表了中国科学院上海营养与健康研究所肖意传课题组与中国科学院上海药物研究所郑明月研究员的合作研究论文“Cytoplasmic DNA sensing by KU complex in aged CD4+ T cell potentiates T cell activation and aging-related autoimmune inflammation”。该研究揭示KU复合物介导CD4+ T细胞中的DNA感知,进而介导衰老相关自身免疫病的调控机制。
人口老龄化是我国乃至世界目前面临的重大社会问题,随着年龄的增大,正常机体会表现为衰老的状态,而免疫系统的衰老是其中突出和重要的问题,其也是老年个体易发慢性炎症与自身免疫病的重要原因。T细胞介导的适应性免疫是机体诱发自身免疫性炎症的关键驱动力,虽然衰老引起的胸腺萎缩会导致初始T细胞输出的减少,然而老年个体外周T细胞的数量并没有减少,其原因是由于外周T细胞在衰老的状态下会发生稳态增殖与活化,然而,衰老诱导T细胞稳态增殖进而促进自身免疫性炎症发生发展的具体调控机制尚不清楚。
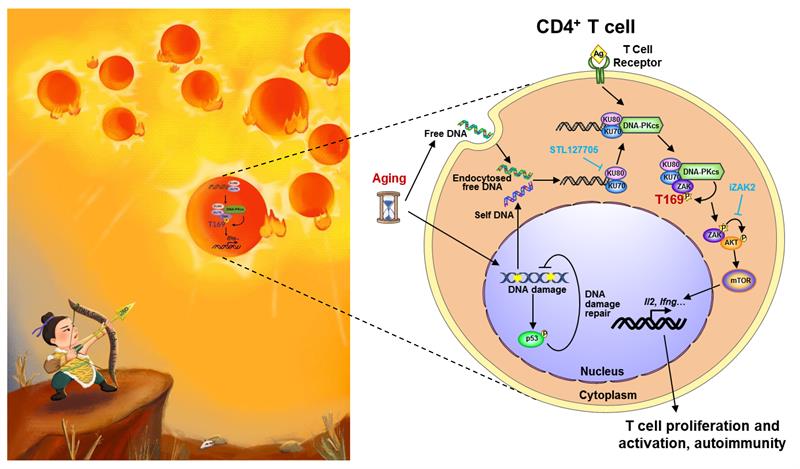
在本研究中,研究人员发现在老年小鼠和人的CD4+ T细胞胞质中存在DNA大量累积的现象,且这些积累的DNA会促进TCR诱导的CD4+ T细胞的增殖与活化,说明T细胞自身会通过DNA感知而促进其功能活化。接着通过质谱结合免疫印迹技术筛选与T细胞中与细胞质DNA结合的蛋白,发现T细胞中DNA并不与cGAS,而是与KU复合物(KU70/KU80)进行结合。如果利用小分子抑制剂STL127705阻断KU复合物与DNA的结合,则显著抑制了DNA诱导的CD4+ T细胞的增殖与活化,进而缓解了老年小鼠自身免疫性炎症的发生发展,说明DNA诱导的T细胞功能活化确实是通过KU复合物感知DNA介导的。通常情况下,KU复合物与DNA依赖的蛋白激酶的催化亚基(DNA-PKcs)一起在细胞核中介导的DNA损伤修复。此研究发现,KU复合物在T细胞的细胞质中大量表达,其在CD4+ T细胞中识别DNA后可促进DNA-PKcs的磷酸化激活,进而介导ZAK的T169位点的磷酸化,活化的ZAK再通过磷酸化AKT激活下游mTOR通路,从而增强了CD4+ T细胞的增殖和活化。因此,CD4+ T细胞中KU复合物介导的DNA感知通路的激活是导致老年小鼠自身免疫性炎症的发生发展的关键机制。
为了探索干预这一新发现的DNA感知通路进而抑制衰老相关自身免疫性炎症的治疗策略,研究人员利用热量限制(CR)或模拟间歇性进食(FMD)处理老年小鼠,发现这两种节食模式都能显著地降低老年小鼠CD4+ T细胞的DNA损伤和细胞质DNA累积,从而抑制了ZAK-T169位点的磷酸化以及下游AKT/mTOR信号的激活,最终抑制了CD4+ T细胞的活化和衰老相关自身免疫病症状。进一步的,基于DNA感知通路中鉴定到的关键蛋白激酶ZAK,研究人员利用深度学习结合分子模拟的方法从大约13万个化合物库中筛选获得了可特异性抑制ZAK激酶活性的小分子化合物iZAK2,发现iZAK2可有效地抑制DNA诱导的CD4+ T细胞增殖活化,由此缓解了老年小鼠自身免疫病的病理症状。
综上所述,该研究揭示了衰老CD4+ T细胞中不依赖于cGAS/STING的DNA感知信号通路,其可促进T细胞的活化和增殖并导致衰老相关自身免疫病的发生发展。进一步研究和开发阻断T细胞中DNA感知信号传导的抑制剂可能有利于临床治疗衰老相关的自身免疫性疾病。该论文发表后,Immunity杂志同期还以Preview的形式介绍并评论了此研究发现,认为发现了一个新型的感知T细胞胞质DNA的KU感受器。
中国科学院上海营养与健康研究所博士生王艳为该论文的第一作者,肖意传研究员和郑明月研究员为论文的共同通讯作者。这项工作得到了武汉大学舒红兵教授和钟波教授、国家蛋白质中心(北京)李涛教授、浙江大学徐平龙教授、中科院上海巴斯德研究所肖晖研究员、同济大学戈宝学教授以及西湖大学常兴教授的大力支持与帮助。该研究还得到了科技部、国家自然科学基金委及中国科学院等项目的资助,同时也得到了中国科学院上海营养与健康研究所公共技术平台和动物平台的支持。
原文链接:https://www.cell.com/immunity/fulltext/S1074-7613(21)00069-8
人口老龄化是我国乃至世界目前面临的重大社会问题,随着年龄的增大,正常机体会表现为衰老的状态,而免疫系统的衰老是其中突出和重要的问题,其也是老年个体易发慢性炎症与自身免疫病的重要原因。T细胞介导的适应性免疫是机体诱发自身免疫性炎症的关键驱动力,虽然衰老引起的胸腺萎缩会导致初始T细胞输出的减少,然而老年个体外周T细胞的数量并没有减少,其原因是由于外周T细胞在衰老的状态下会发生稳态增殖与活化,然而,衰老诱导T细胞稳态增殖进而促进自身免疫性炎症发生发展的具体调控机制尚不清楚。
在本研究中,研究人员发现在老年小鼠和人的CD4+ T细胞胞质中存在DNA大量累积的现象,且这些积累的DNA会促进TCR诱导的CD4+ T细胞的增殖与活化,说明T细胞自身会通过DNA感知而促进其功能活化。接着通过质谱结合免疫印迹技术筛选与T细胞中与细胞质DNA结合的蛋白,发现T细胞中DNA并不与cGAS,而是与KU复合物(KU70/KU80)进行结合。如果利用小分子抑制剂STL127705阻断KU复合物与DNA的结合,则显著抑制了DNA诱导的CD4+ T细胞的增殖与活化,进而缓解了老年小鼠自身免疫性炎症的发生发展,说明DNA诱导的T细胞功能活化确实是通过KU复合物感知DNA介导的。通常情况下,KU复合物与DNA依赖的蛋白激酶的催化亚基(DNA-PKcs)一起在细胞核中介导的DNA损伤修复。此研究发现,KU复合物在T细胞的细胞质中大量表达,其在CD4+ T细胞中识别DNA后可促进DNA-PKcs的磷酸化激活,进而介导ZAK的T169位点的磷酸化,活化的ZAK再通过磷酸化AKT激活下游mTOR通路,从而增强了CD4+ T细胞的增殖和活化。因此,CD4+ T细胞中KU复合物介导的DNA感知通路的激活是导致老年小鼠自身免疫性炎症的发生发展的关键机制。
为了探索干预这一新发现的DNA感知通路进而抑制衰老相关自身免疫性炎症的治疗策略,研究人员利用热量限制(CR)或模拟间歇性进食(FMD)处理老年小鼠,发现这两种节食模式都能显著地降低老年小鼠CD4+ T细胞的DNA损伤和细胞质DNA累积,从而抑制了ZAK-T169位点的磷酸化以及下游AKT/mTOR信号的激活,最终抑制了CD4+ T细胞的活化和衰老相关自身免疫病症状。进一步的,基于DNA感知通路中鉴定到的关键蛋白激酶ZAK,研究人员利用深度学习结合分子模拟的方法从大约13万个化合物库中筛选获得了可特异性抑制ZAK激酶活性的小分子化合物iZAK2,发现iZAK2可有效地抑制DNA诱导的CD4+ T细胞增殖活化,由此缓解了老年小鼠自身免疫病的病理症状。

衰老CD4+ T细胞中DNA感知促进其活化与自身免疫性炎症的卡通与机制示意图
综上所述,该研究揭示了衰老CD4+ T细胞中不依赖于cGAS/STING的DNA感知信号通路,其可促进T细胞的活化和增殖并导致衰老相关自身免疫病的发生发展。进一步研究和开发阻断T细胞中DNA感知信号传导的抑制剂可能有利于临床治疗衰老相关的自身免疫性疾病。该论文发表后,Immunity杂志同期还以Preview的形式介绍并评论了此研究发现,认为发现了一个新型的感知T细胞胞质DNA的KU感受器。
中国科学院上海营养与健康研究所博士生王艳为该论文的第一作者,肖意传研究员和郑明月研究员为论文的共同通讯作者。这项工作得到了武汉大学舒红兵教授和钟波教授、国家蛋白质中心(北京)李涛教授、浙江大学徐平龙教授、中科院上海巴斯德研究所肖晖研究员、同济大学戈宝学教授以及西湖大学常兴教授的大力支持与帮助。该研究还得到了科技部、国家自然科学基金委及中国科学院等项目的资助,同时也得到了中国科学院上海营养与健康研究所公共技术平台和动物平台的支持。
原文链接:https://www.cell.com/immunity/fulltext/S1074-7613(21)00069-8
