学术动态
高平/张华凤团队合作发现肌肽通过维持胞内pH稳态及溶酶体活性促进肿瘤免疫逃逸的新机制
作者:严荣辉 来源自:中国免疫学会 点击数:4571 发布时间:2024-03-28
100年前,德国科学家Otto Warburg发现, 与正常细胞相比,即使在有氧气存在的条件下,肿瘤细胞也倾向于吸收大量葡萄糖利用糖酵解的方式供能,这一现象也被称为“Warburg 效应”。肿瘤细胞在利用Warburg效应供能的同时,也导致大量酸性产物乳酸的生成,造成肿瘤的酸性微环境,并长远地影响肿瘤及其微环境内的免疫细胞。有趣的是,尽管在低氧下Warburg 效应增强,肿瘤细胞外部形成酸性微环境,但肿瘤细胞内的pH却维持在7.2左右的生理范围,其背后的机制及意义目前并不清楚。
早期的研究表明,通过细胞膜上的离子通道或者转运体,可以将细胞内的H+释放到胞外(如单羧酸转运体,MCTs)。然而,这忽视了蕴藏其中的一个关键问题:糖酵解反应生成的乳酸,在胞浆中主要以乳酸根和游离H+的形式存在(乳酸pKa= 4.14),胞浆中大量蛋白质侧链基团带有负电荷,游离的H+很容易被这些带负电荷的基团吸引,而不能在胞浆内快速地自由移动,而参与释放胞内H+的离子通道或者转运体主要定位于细胞膜上。因此,胞浆中糖酵解产生的大量H+是如何移动到细胞膜附近,并进一步被释放出去,目前并不清楚。早期的研究中,生理学家发现有一些物质在不同pH条件下能够中和H+正电荷,充当H+的穿梭载体,帮助它们在负电荷环境中自由移动,这些物质具有pH缓冲作用,也被称为可移动缓冲物(mobile buffer)。类似的可移动缓冲物质在肿瘤细胞中是否存在,如何发挥作用,目前鲜有报道。此外,近期研究发现胞内pH参与调控了多种生物学过程,比如胚胎发育、昼夜节律、肌肉重塑等,而关于胞内pH是否参与调控肿瘤进展,尤其是肿瘤免疫仍不清楚。
2024年1月4日, 南方医科大学/广东省人民医院高平课题组与中国科学技术大学张华凤课题组合作在Nature Immunology期刊上发表题为“Carnosine regulation of intracellular pH homeostasis promotes lysosome-dependent tumor immunoevasion”的研究论文。该研究发现当肿瘤细胞处于缺氧条件,Warburg效应增强,产生大量乳酸时,肿瘤细胞通过增强可移动缓冲物质肌肽的合成来抵抗胞内的过度酸化,从而维持胞内pH稳态,调节溶酶体在细胞内的定位和功能,并进一步参与调控免疫检查点蛋白Galectin-9的表达,最终促进肿瘤免疫逃逸和肝癌进展。
在本项研究中,研究人员首先检测低氧条件下,肿瘤细胞内潜在的可移动缓冲物质含量的变化,并结合这些物质的生化特点(pKa)分析, 发现肌肽是生理环境中最佳(pKa=6.76, 最接近生理pH)、变化最显著的可移动缓冲物, 并进一步证实了肌肽参与维持胞内pH稳态。具体的机制主要包括:1) 肌肽作为可移动缓冲物质能够与胞浆游离的H+结合,减缓胞内pH的波动; 2) 一部分肌肽通过在胞内 pH相对较低的区域(如糖酵解发生的区域)和pH相对较高的区域(如细胞膜附近区域)之间切换其质子化状态,充当循环移动质子载体,从而为位于细胞膜上的离子通道或转运蛋白提供底物H+,加速细胞质H+向胞外运输;3)细胞内肌肽还可以通过SLC15A1-4转运体直接将细胞质中H+转运到内体/溶酶体以及细胞外。作者还探究了低氧导致肿瘤细胞中肌肽合成增多的原因,发现低氧条件下肿瘤细胞中的肌肽主要是由肌肽合酶2(CARNS2)催化合成的,CARNS2是本项工作新发现的一种肌肽合成酶,主要表达在肝癌细胞或组织中,是由低氧微环境诱发可变剪切生成的。而之前报道的肌肽合酶1(CARNS1)主要表达在正常肌肉及脑组织中。
通过共聚焦等实验,研究人员进一步发现,操纵细胞内CARNS2的蛋白水平或者肌肽的含量,能够改变溶酶体在细胞中的定位,进而影响其酸化和功能。考虑到溶酶体参与了细胞内蛋白质的降解过程,研究人员通过溶酶体蛋白质组学筛选到在低氧条件下受肌肽通路显著调控的关键分子NFX1。NFX1是一个转录抑制因子,有报道其参与调控巨噬细胞的免疫反应,但在肿瘤免疫中发挥怎样的功能目前还未被挖掘。为了探讨胞内pH与肿瘤免疫之间的关联,研究人员通过RNA-Seq等实验进一步分析了NFX1的下游通路,发现NFX1能够显著抑制免疫检查点蛋白Galectin-9的表达。作者在同种移植瘤以及YAP5SA诱导的原位小鼠肝癌模型中,分析CARNS2-NFX1-Galectin-9通路对肿瘤免疫的影响,研究结果显示,敲低CARNS2能够显著上调肿瘤浸润T细胞的数量,并且T细胞耗竭减少,效应功能增强。这些研究结果表明,肿瘤细胞中的肌肽通过维持胞内pH稳态,从而维持溶酶体在细胞内的定位及功能,降解转录抑制因子NFX1,进而促进Galectin-9的表达,最终实现肿瘤细胞的免疫逃逸。临床实验数据也表明CARNS2/NFX1/Galectin-9调节轴的异常激活与肝癌的发生发展高度相关。
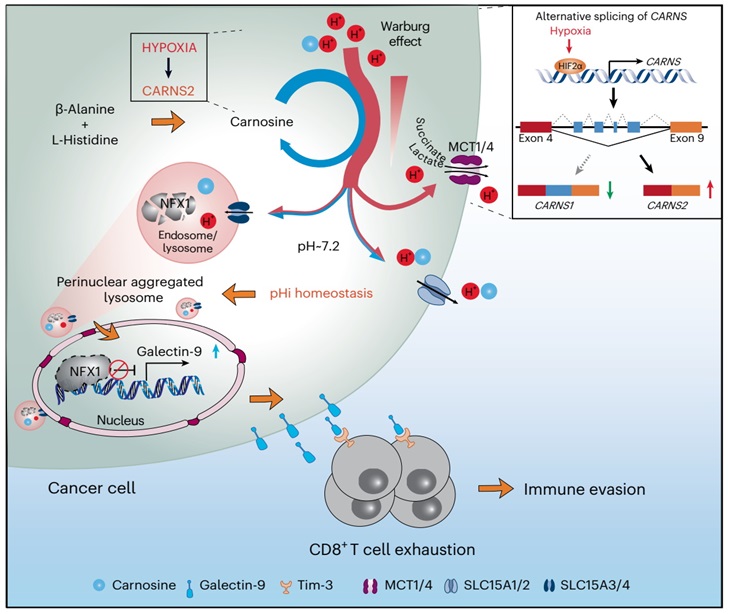
“Warburg 效应”是100年前由德国科学家Otto Warburg提出的里程碑式的重要发现,长期以来的焦点集中于为什么肿瘤细胞会以如此浪费的能量代谢方式获得增殖优势。本研究则以“Warburg 效应”,即有氧糖酵解,产生的乳酸为切入点,探讨肿瘤细胞内pH稳态维持的机制,揭示胞内pH稳态、溶酶体功能与免疫逃逸之间的关联,有重要的科学价值,并为通过靶向干预胞内pH及溶酶体功能、重塑免疫微环境来改善肿瘤免疫治疗提供了潜在的新思路和新策略。
中国科学技术大学严荣辉博士、张平根博士为论文的共同第一作者;高平教授、张华凤教授为论文的共同通讯作者。本项研究得到了中国科学技术大学仓春蕾教授团队以及中国科学技术大学附属第一医院荚卫东教授的指导和大力帮助。这项工作获得了国家基金委、科技部、中科院、合肥大健康研究院等项目的资助。
原文链接:https://www.nature.com/articles/s41590-023-01719-3
早期的研究表明,通过细胞膜上的离子通道或者转运体,可以将细胞内的H+释放到胞外(如单羧酸转运体,MCTs)。然而,这忽视了蕴藏其中的一个关键问题:糖酵解反应生成的乳酸,在胞浆中主要以乳酸根和游离H+的形式存在(乳酸pKa= 4.14),胞浆中大量蛋白质侧链基团带有负电荷,游离的H+很容易被这些带负电荷的基团吸引,而不能在胞浆内快速地自由移动,而参与释放胞内H+的离子通道或者转运体主要定位于细胞膜上。因此,胞浆中糖酵解产生的大量H+是如何移动到细胞膜附近,并进一步被释放出去,目前并不清楚。早期的研究中,生理学家发现有一些物质在不同pH条件下能够中和H+正电荷,充当H+的穿梭载体,帮助它们在负电荷环境中自由移动,这些物质具有pH缓冲作用,也被称为可移动缓冲物(mobile buffer)。类似的可移动缓冲物质在肿瘤细胞中是否存在,如何发挥作用,目前鲜有报道。此外,近期研究发现胞内pH参与调控了多种生物学过程,比如胚胎发育、昼夜节律、肌肉重塑等,而关于胞内pH是否参与调控肿瘤进展,尤其是肿瘤免疫仍不清楚。
2024年1月4日, 南方医科大学/广东省人民医院高平课题组与中国科学技术大学张华凤课题组合作在Nature Immunology期刊上发表题为“Carnosine regulation of intracellular pH homeostasis promotes lysosome-dependent tumor immunoevasion”的研究论文。该研究发现当肿瘤细胞处于缺氧条件,Warburg效应增强,产生大量乳酸时,肿瘤细胞通过增强可移动缓冲物质肌肽的合成来抵抗胞内的过度酸化,从而维持胞内pH稳态,调节溶酶体在细胞内的定位和功能,并进一步参与调控免疫检查点蛋白Galectin-9的表达,最终促进肿瘤免疫逃逸和肝癌进展。
在本项研究中,研究人员首先检测低氧条件下,肿瘤细胞内潜在的可移动缓冲物质含量的变化,并结合这些物质的生化特点(pKa)分析, 发现肌肽是生理环境中最佳(pKa=6.76, 最接近生理pH)、变化最显著的可移动缓冲物, 并进一步证实了肌肽参与维持胞内pH稳态。具体的机制主要包括:1) 肌肽作为可移动缓冲物质能够与胞浆游离的H+结合,减缓胞内pH的波动; 2) 一部分肌肽通过在胞内 pH相对较低的区域(如糖酵解发生的区域)和pH相对较高的区域(如细胞膜附近区域)之间切换其质子化状态,充当循环移动质子载体,从而为位于细胞膜上的离子通道或转运蛋白提供底物H+,加速细胞质H+向胞外运输;3)细胞内肌肽还可以通过SLC15A1-4转运体直接将细胞质中H+转运到内体/溶酶体以及细胞外。作者还探究了低氧导致肿瘤细胞中肌肽合成增多的原因,发现低氧条件下肿瘤细胞中的肌肽主要是由肌肽合酶2(CARNS2)催化合成的,CARNS2是本项工作新发现的一种肌肽合成酶,主要表达在肝癌细胞或组织中,是由低氧微环境诱发可变剪切生成的。而之前报道的肌肽合酶1(CARNS1)主要表达在正常肌肉及脑组织中。
通过共聚焦等实验,研究人员进一步发现,操纵细胞内CARNS2的蛋白水平或者肌肽的含量,能够改变溶酶体在细胞中的定位,进而影响其酸化和功能。考虑到溶酶体参与了细胞内蛋白质的降解过程,研究人员通过溶酶体蛋白质组学筛选到在低氧条件下受肌肽通路显著调控的关键分子NFX1。NFX1是一个转录抑制因子,有报道其参与调控巨噬细胞的免疫反应,但在肿瘤免疫中发挥怎样的功能目前还未被挖掘。为了探讨胞内pH与肿瘤免疫之间的关联,研究人员通过RNA-Seq等实验进一步分析了NFX1的下游通路,发现NFX1能够显著抑制免疫检查点蛋白Galectin-9的表达。作者在同种移植瘤以及YAP5SA诱导的原位小鼠肝癌模型中,分析CARNS2-NFX1-Galectin-9通路对肿瘤免疫的影响,研究结果显示,敲低CARNS2能够显著上调肿瘤浸润T细胞的数量,并且T细胞耗竭减少,效应功能增强。这些研究结果表明,肿瘤细胞中的肌肽通过维持胞内pH稳态,从而维持溶酶体在细胞内的定位及功能,降解转录抑制因子NFX1,进而促进Galectin-9的表达,最终实现肿瘤细胞的免疫逃逸。临床实验数据也表明CARNS2/NFX1/Galectin-9调节轴的异常激活与肝癌的发生发展高度相关。

肌肽通过维持胞内pH稳态及溶酶体活性促进肿瘤免疫逃逸
“Warburg 效应”是100年前由德国科学家Otto Warburg提出的里程碑式的重要发现,长期以来的焦点集中于为什么肿瘤细胞会以如此浪费的能量代谢方式获得增殖优势。本研究则以“Warburg 效应”,即有氧糖酵解,产生的乳酸为切入点,探讨肿瘤细胞内pH稳态维持的机制,揭示胞内pH稳态、溶酶体功能与免疫逃逸之间的关联,有重要的科学价值,并为通过靶向干预胞内pH及溶酶体功能、重塑免疫微环境来改善肿瘤免疫治疗提供了潜在的新思路和新策略。
中国科学技术大学严荣辉博士、张平根博士为论文的共同第一作者;高平教授、张华凤教授为论文的共同通讯作者。本项研究得到了中国科学技术大学仓春蕾教授团队以及中国科学技术大学附属第一医院荚卫东教授的指导和大力帮助。这项工作获得了国家基金委、科技部、中科院、合肥大健康研究院等项目的资助。
原文链接:https://www.nature.com/articles/s41590-023-01719-3
