学术动态
邵峰院士团队发现GSDMB被颗粒酶激活进而诱导靶细胞发生焦亡
作者:邵峰 来源自:中国免疫学会 点击数:81568 发布时间:2020-06-20
2020年5月29日,北京生命科学研究所邵峰院士团队在国际顶级杂志Science发表题为Granzyme A From Cytotoxic Lymphocytes Cleaves GSDMB to Trigger Pyroptosis in Target Cells的成果,首次揭示了细胞毒性淋巴细胞所分泌的颗粒酶 A(Granzyme A,GZMA)通过切割 Gasdermin B (GSDMB) 以诱发细胞焦亡的重要机制,为肿瘤免疫提供了新思路。
细胞毒性淋巴细胞是一类主要的免疫效应细胞,在机体清除病毒感染或者癌变的细胞过程中发挥着重要作用。细胞毒性淋巴细胞介导的免疫作用主要依赖于颗粒酶。尽管尚不完全了解其潜在机制,但研究者认为颗粒酶通过诱导细胞凋亡杀死靶细胞。了解细胞毒性淋巴细胞如何利用这条途径杀死靶细胞是免疫学的核心问题,特别是考虑到细胞毒性T淋巴细胞(CTLs)在癌症免疫治疗中的关键作用。
邵峰团队建立了NK-92MI细胞杀伤实验模型,发现NK细胞通过切割GSDMB诱导GSDMB依赖性的细胞焦亡。进一步的体外生化研究表明,GZMA通过位点特异性切割激活了GSDMB,从而释放其打孔活性结构域,导致细胞焦亡。重要的是,邵峰团队发现GZMA-GSDMB通路介导的细胞焦亡仅需要GSDMB和GZMA参与。有趣的是,干扰素和TNF-α均可上调GSDMB表达并促进GZMA诱导的细胞焦亡。此外,GZMA-GSDMB通路对CTLs介导的焦亡性杀伤也至关重要。通过小鼠肿瘤模型,邵峰团队证明了GZMA-GSDMB通路促进了小鼠对肿瘤的清除。
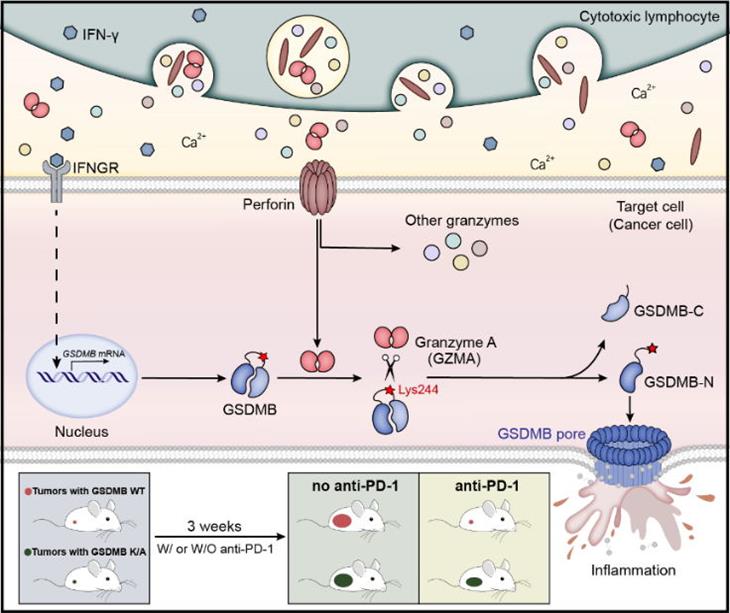
细胞毒性淋巴细胞所分泌的GZMA激活GSDMB,导致细胞焦亡
综上,邵峰团队揭示了细胞毒性淋巴细胞介导的免疫新机制。重要的是,这项研究发现GSDMB作用于颗粒酶下游,这突显了诸如caspase之类的蛋白裂解酶以及颗粒酶本质上并不是细胞死亡执行蛋白的事实,Gasdermin蛋白家族才是细胞焦亡的直接执行者。这提示着不同的靶细胞,即便当它们被相同类型的细胞毒性淋巴细胞类似地识别时,也可能经历不同类型的细胞死亡。因此,未来对淋巴细胞介导的免疫反应的研究应当更多地关注靶细胞内的死亡执行相关事件,而不是细胞表面分子,比如PD-1。
北京生命科学研究所的邵峰院士为本文通讯作者,该实验室的周志伟博士和何华斌博士为本文共同第一作者。
文章链接:https://science.sciencemag.org/content/368/6494/eaaz7548.long
细胞毒性淋巴细胞是一类主要的免疫效应细胞,在机体清除病毒感染或者癌变的细胞过程中发挥着重要作用。细胞毒性淋巴细胞介导的免疫作用主要依赖于颗粒酶。尽管尚不完全了解其潜在机制,但研究者认为颗粒酶通过诱导细胞凋亡杀死靶细胞。了解细胞毒性淋巴细胞如何利用这条途径杀死靶细胞是免疫学的核心问题,特别是考虑到细胞毒性T淋巴细胞(CTLs)在癌症免疫治疗中的关键作用。
邵峰团队建立了NK-92MI细胞杀伤实验模型,发现NK细胞通过切割GSDMB诱导GSDMB依赖性的细胞焦亡。进一步的体外生化研究表明,GZMA通过位点特异性切割激活了GSDMB,从而释放其打孔活性结构域,导致细胞焦亡。重要的是,邵峰团队发现GZMA-GSDMB通路介导的细胞焦亡仅需要GSDMB和GZMA参与。有趣的是,干扰素和TNF-α均可上调GSDMB表达并促进GZMA诱导的细胞焦亡。此外,GZMA-GSDMB通路对CTLs介导的焦亡性杀伤也至关重要。通过小鼠肿瘤模型,邵峰团队证明了GZMA-GSDMB通路促进了小鼠对肿瘤的清除。

细胞毒性淋巴细胞所分泌的GZMA激活GSDMB,导致细胞焦亡
综上,邵峰团队揭示了细胞毒性淋巴细胞介导的免疫新机制。重要的是,这项研究发现GSDMB作用于颗粒酶下游,这突显了诸如caspase之类的蛋白裂解酶以及颗粒酶本质上并不是细胞死亡执行蛋白的事实,Gasdermin蛋白家族才是细胞焦亡的直接执行者。这提示着不同的靶细胞,即便当它们被相同类型的细胞毒性淋巴细胞类似地识别时,也可能经历不同类型的细胞死亡。因此,未来对淋巴细胞介导的免疫反应的研究应当更多地关注靶细胞内的死亡执行相关事件,而不是细胞表面分子,比如PD-1。
北京生命科学研究所的邵峰院士为本文通讯作者,该实验室的周志伟博士和何华斌博士为本文共同第一作者。
文章链接:https://science.sciencemag.org/content/368/6494/eaaz7548.long
