学术动态
山东大学赵伟团队《Nat Immunol》发文报道脂质氧化还原稳态在cGAS-STING通路激活中的作用
作者:赵伟 来源自:中国免疫学会 点击数:76495 发布时间:2020-07-10
cGAS是重要的胞浆DNA受体,识别病毒DNA和胞浆中的自身DNA后,合成第二信使--环鸟腺苷酸(cGAMP);cGAMP激活STING ,活化的STING从内质网向高尔基体的转位,进而激活TBK1及IRF3介导的天然免疫信号通路。氧化还原稳态是机体对病毒感染及肿瘤等应激反应的一种生理校正反应,在生命活动中发挥重要作用。然而,氧化还原稳态与DNA识别信号通路的相互作用,特别是脂质氧化还原稳态对cGAS-STING介导的天然免疫启动的影响,并不清楚。
2020年6月15日,山东大学赵伟教授团队在《Nature Immunology》杂志发表题为“Redox homeostasis maintained by GPX4 facilitates STING activation”的研究论文。该研究将氧化还原稳态与DNA识别信号通路联系起来,揭示了谷胱甘肽过氧化物酶4(GPX4)维持的脂质氧化还原稳态在cGAS介导的天然免疫启动中的关键作用。
氧化还原稳态是所有生命活动的重要组成部分。过氧化脂质生成增多破坏氧化还原稳态,与多种疾病密切相关,包括病毒性疾病和肿瘤等。该研究发现,GPX4维持的脂质氧化还原稳态是STING激活的必需因素。GPX4缺失通过增强脂质过氧化,特异性抑制cGAS-STING介导的DNA识别通路,并抑制DNA病毒HSV-1感染诱导的IFN-β表达及抗病毒反应,而对RLR介导的RNA识别通路和TLR通路活化均没有影响。病毒感染导致胞内脂质过氧化水平升高,产生4-HNE等脂质过氧化代谢产物从而抑制STING活化;GPX4缺失可进一步促进4-HNE产生、抑制STING介导的抗DNA病毒免疫反应。研究接下来解析了脂质过氧化代谢产物4-HNE抑制STING活化的精确机制,该研究发现4-HNE与STING的第88位半胱氨酸(C88)发生Michael加成反应形成羰基化修饰,从而抑制STING棕榈酰化和由内质网向高尔基体的转位,阻断STING介导的天然免疫反应。
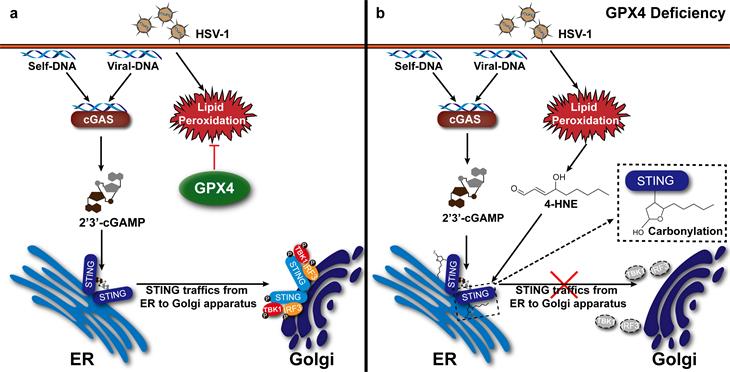
综上所述,该研究以DNA病毒HSV-1感染为模型,揭示了病毒如何调控脂质过氧化抑制宿主抗病毒免疫反应、实现免疫逃逸的机制。该STING活化的新机制,深化了对DNA识别通路及天然免疫启动的认知。同时,提供了一种通过调控GPX4活性和脂质过氧化来调节STING激活的新策略,为STING活化失衡相关疾病的防治提供了新的靶标。
山东大学基础医学院赵伟教授为本文通讯作者,博士研究生贾木天为本文第一作者。该研究得到了国家自然科学基金、国家重点研发计划、英国医学科学院牛顿高级学者项目、山东大学攀登计划创新团队等经费支持。
文章链接:https://www.nature.com/articles/s41590-020-0699-0
2020年6月15日,山东大学赵伟教授团队在《Nature Immunology》杂志发表题为“Redox homeostasis maintained by GPX4 facilitates STING activation”的研究论文。该研究将氧化还原稳态与DNA识别信号通路联系起来,揭示了谷胱甘肽过氧化物酶4(GPX4)维持的脂质氧化还原稳态在cGAS介导的天然免疫启动中的关键作用。
氧化还原稳态是所有生命活动的重要组成部分。过氧化脂质生成增多破坏氧化还原稳态,与多种疾病密切相关,包括病毒性疾病和肿瘤等。该研究发现,GPX4维持的脂质氧化还原稳态是STING激活的必需因素。GPX4缺失通过增强脂质过氧化,特异性抑制cGAS-STING介导的DNA识别通路,并抑制DNA病毒HSV-1感染诱导的IFN-β表达及抗病毒反应,而对RLR介导的RNA识别通路和TLR通路活化均没有影响。病毒感染导致胞内脂质过氧化水平升高,产生4-HNE等脂质过氧化代谢产物从而抑制STING活化;GPX4缺失可进一步促进4-HNE产生、抑制STING介导的抗DNA病毒免疫反应。研究接下来解析了脂质过氧化代谢产物4-HNE抑制STING活化的精确机制,该研究发现4-HNE与STING的第88位半胱氨酸(C88)发生Michael加成反应形成羰基化修饰,从而抑制STING棕榈酰化和由内质网向高尔基体的转位,阻断STING介导的天然免疫反应。

综上所述,该研究以DNA病毒HSV-1感染为模型,揭示了病毒如何调控脂质过氧化抑制宿主抗病毒免疫反应、实现免疫逃逸的机制。该STING活化的新机制,深化了对DNA识别通路及天然免疫启动的认知。同时,提供了一种通过调控GPX4活性和脂质过氧化来调节STING激活的新策略,为STING活化失衡相关疾病的防治提供了新的靶标。
山东大学基础医学院赵伟教授为本文通讯作者,博士研究生贾木天为本文第一作者。该研究得到了国家自然科学基金、国家重点研发计划、英国医学科学院牛顿高级学者项目、山东大学攀登计划创新团队等经费支持。
文章链接:https://www.nature.com/articles/s41590-020-0699-0
