学术动态
彭勃/曹立/饶艳霞团队《Science》首次实现小胶质细胞替换临床治疗,成功阻断致死性脑病ALSP病程进展
作者:彭勃 来源自:中国免疫学会 点击数:10480 发布时间:2025-07-11
2025年7月10日,上海的研究团队在《Science》期刊发表题为“Microglia replacement halts the progression of microgliopathy in mice and humans”的突破性研究成果:通过替换中枢神经系统中的致病性小胶质细胞,成功阻断了CSF1R相关脑白质病(ALSP)在动物模型和人类患者中的病程进展。该研究还首次揭示,传统骨髓细胞移植(tBMT)在ALSP特定病理背景下,机制上等效于研究团队开发的小胶质细胞替换技术Mr BMT,能够实现高效细胞替换和神经功能改善。这项成果构成了迄今唯一获得机制验证和临床疗效证据支持的ALSP治疗方案,标志着我国在小胶质细胞干预领域处于国际领先地位(图1)。
彭勃、曹立、饶艳霞是该研究工作的通讯作者;邬静莹、王亚飞、李小钰、欧阳霈是该研究工作的共同第一作者。

图1 论文首页截图
ALSP是一种进展迅速的致死性疾病
成人起病轴突膨胀伴色素胶质细胞脑白质病(adult-onset leukoencephalopathy with axonal spheroids and pigmented glia, ALSP)是一种由CSF1R基因突变引发小胶质细胞功能障碍的遗传性白质脑病。患者通常在成年后发病,病情进展迅速,主要表现为小胶质细胞数目减少、脑白质广泛脱髓鞘、轴突肿胀、轴索球样变、脑钙化、认知障碍和进行性运动能力退化,最终导致严重神经功能丧失。在我国,ALSP在患者临床发病后的平均生存期仅为3-6.8年,至今尚无有效的临床方案可以治疗或减缓该疾病的发生发展。
首次构建模拟人类ALSP病理特征的动物模型
ALSP发病机制以小胶质细胞功能异常为核心,但长期以来,研究所依赖的动物模型未能真实再现其关键病理特征。例如,CSF1R杂合缺失模型CSF1RWT/KO不仅不能表现出脑白质病变,反而出现小胶质细胞数量升高,且无明显运动障碍或脑钙化;而另一类CSF1RΔFIRE/ΔFIRE小鼠模型中小胶质细胞完全缺失,不仅不能反映病理性小胶质细胞在脑内的作用,更与ALSP患者“小胶质细胞数量减少但未消失”的临床病理明显不符。因此,当前广泛使用的CSF1RWT/KO模型和CSF1RΔFIRE/ΔFIRE模型均无法满足机制研究与疗效验证的需求,严重制约了有效治疗策略的开发。
在本研究中,团队基于全球ALSP患者的突变谱,建立了两种携带CSF1R热点突变的小鼠模型(I792T和E631K),全面复现了ALSP的病理学和行为学特征,首次为ALSP疾病的研究提供了可靠的动物疾病模型。
中国团队率先提出并实现小胶质细胞替换策略
2020年,复旦大学彭勃教授团队在《Cell Reports》全球首次提出并实现“以小胶质细胞替换为核心的中枢治疗策略”,系统开发了三种替换路径:基于骨髓供体的Mr BMT、基于外周血供体的Mr PB,以及局部定点移植的Mr MT(图2)(PMID: 33238120),并将详细的操作方案向全领域公开。这一系列策略突破了传统骨髓细胞移植无法替换脑内小胶质细胞的瓶颈,构建了首个可操作、机制清晰的小胶质细胞干预体系。进一步通过该策略,提出了MISTER(microglia intervention strategy for therapy and enhancement by replacement)概念,用于开展神经系统疾病治疗的新型细胞疗法。
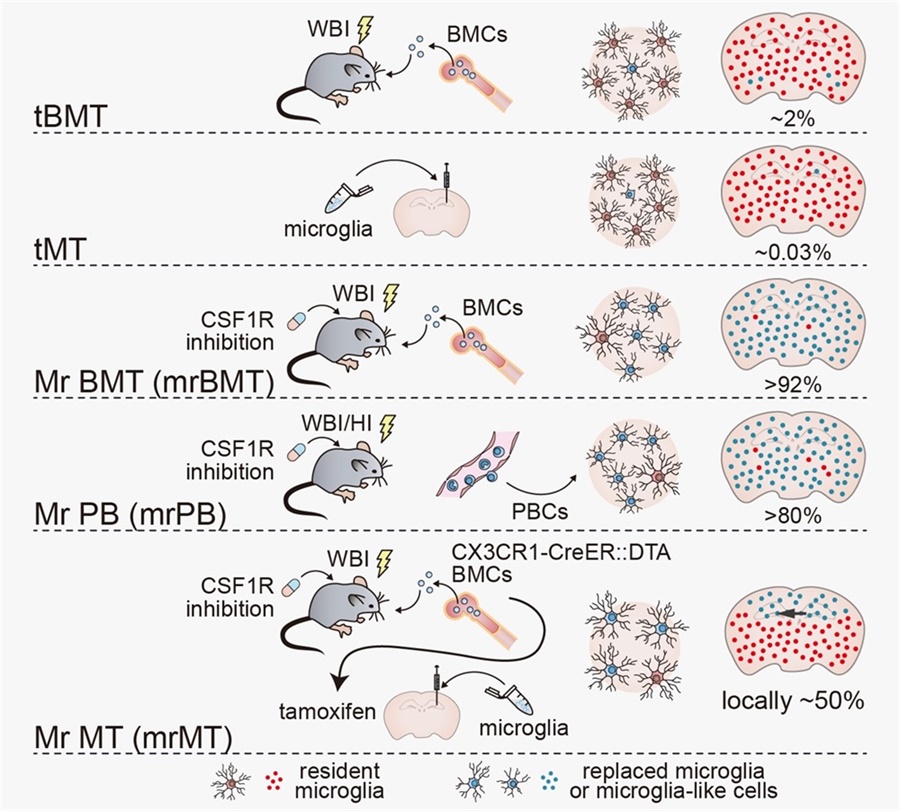
图2 全球首次实现的小胶质细胞替换策略
构建精准模型并验证替换疗效
在本研究中,团队在新建立的I792T和E631K小鼠模型中实施Mr BMT干预,以CSF1R正常供体细胞成功替换了超过90%的脑内小胶质细胞,并观察到髓鞘修复、轴突保护、神经电传导增强以及运动与认知能力恢复等一系列治疗效应(图3)。转录组分析进一步揭示替换细胞重塑了CSF1R相关信号通路和多个神经发育、免疫稳态调控过程,明确了替换治疗的机制基础。
全球首次用于临床,并在人类患者中成功阻断ALSP的病程进展
研究还首次证明,CSF1R缺陷导致的内源小胶质细胞竞争力下降,使得传统骨髓细胞移植(tBMT)可在无辅助药物条件下也实现与Mr BMT相当的小胶质细胞替换效率。ALSP可能是目前已知可通过传统骨髓移植路径实现小胶质细胞替换的唯一神经系统疾病。研究团队进一步在8名确诊ALSP患者中开展基于tBMT的小胶质细胞替换治疗,并完成2年随访。结果显示,患者脑部结构无进展性破坏,PET成像显示小胶质细胞相关葡萄糖代谢显著提升,多个运动和认知功能评分稳定甚至出现改善(图3)。这是全球首次在人类患者中系统验证小胶质细胞替换的临床可行性与长期疗效。该研究也解释了前期被误诊为异染性脑白质营养不良(MLD)的ALSP患者在误诊背景下接受tBMT后病情得到缓解的现象。
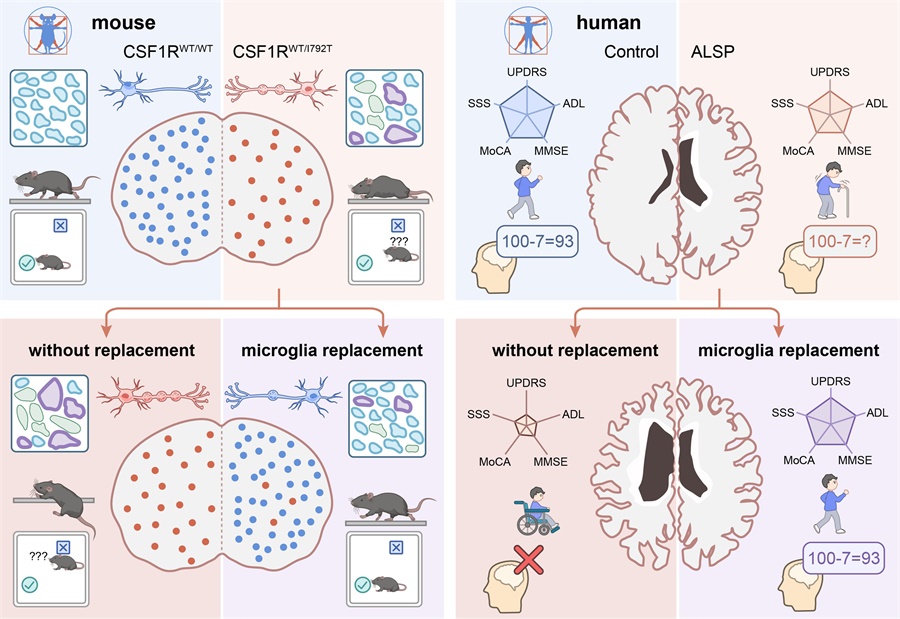
图3 基于小胶质细胞替换的细胞治疗策略,通过修正致病基因突变,成功阻断ALSP在小鼠和人类患者中的发生和发展
美国国家医学院院士、华盛顿大学教授Jonathan Kipnis在《Science》上发表了同期专文评述(Perspective)——“ALSP的遗传学基础在十多年前就已被明确,但迄今仍缺乏针对其根本病因的有效治疗方法。本研究的作者通过以野生型骨髓来源的细胞替换携带CSF1R突变的小胶质细胞,成功地在ALSP的小鼠模型和人类患者中阻止了疾病进展,彰显了小胶质细胞替换疗法的治疗前景。”
原文链接:https://doi.org/10.1126/science.adr1015
彭勃、曹立、饶艳霞是该研究工作的通讯作者;邬静莹、王亚飞、李小钰、欧阳霈是该研究工作的共同第一作者。

图1 论文首页截图
ALSP是一种进展迅速的致死性疾病
成人起病轴突膨胀伴色素胶质细胞脑白质病(adult-onset leukoencephalopathy with axonal spheroids and pigmented glia, ALSP)是一种由CSF1R基因突变引发小胶质细胞功能障碍的遗传性白质脑病。患者通常在成年后发病,病情进展迅速,主要表现为小胶质细胞数目减少、脑白质广泛脱髓鞘、轴突肿胀、轴索球样变、脑钙化、认知障碍和进行性运动能力退化,最终导致严重神经功能丧失。在我国,ALSP在患者临床发病后的平均生存期仅为3-6.8年,至今尚无有效的临床方案可以治疗或减缓该疾病的发生发展。
首次构建模拟人类ALSP病理特征的动物模型
ALSP发病机制以小胶质细胞功能异常为核心,但长期以来,研究所依赖的动物模型未能真实再现其关键病理特征。例如,CSF1R杂合缺失模型CSF1RWT/KO不仅不能表现出脑白质病变,反而出现小胶质细胞数量升高,且无明显运动障碍或脑钙化;而另一类CSF1RΔFIRE/ΔFIRE小鼠模型中小胶质细胞完全缺失,不仅不能反映病理性小胶质细胞在脑内的作用,更与ALSP患者“小胶质细胞数量减少但未消失”的临床病理明显不符。因此,当前广泛使用的CSF1RWT/KO模型和CSF1RΔFIRE/ΔFIRE模型均无法满足机制研究与疗效验证的需求,严重制约了有效治疗策略的开发。
在本研究中,团队基于全球ALSP患者的突变谱,建立了两种携带CSF1R热点突变的小鼠模型(I792T和E631K),全面复现了ALSP的病理学和行为学特征,首次为ALSP疾病的研究提供了可靠的动物疾病模型。
中国团队率先提出并实现小胶质细胞替换策略
2020年,复旦大学彭勃教授团队在《Cell Reports》全球首次提出并实现“以小胶质细胞替换为核心的中枢治疗策略”,系统开发了三种替换路径:基于骨髓供体的Mr BMT、基于外周血供体的Mr PB,以及局部定点移植的Mr MT(图2)(PMID: 33238120),并将详细的操作方案向全领域公开。这一系列策略突破了传统骨髓细胞移植无法替换脑内小胶质细胞的瓶颈,构建了首个可操作、机制清晰的小胶质细胞干预体系。进一步通过该策略,提出了MISTER(microglia intervention strategy for therapy and enhancement by replacement)概念,用于开展神经系统疾病治疗的新型细胞疗法。

图2 全球首次实现的小胶质细胞替换策略
构建精准模型并验证替换疗效
在本研究中,团队在新建立的I792T和E631K小鼠模型中实施Mr BMT干预,以CSF1R正常供体细胞成功替换了超过90%的脑内小胶质细胞,并观察到髓鞘修复、轴突保护、神经电传导增强以及运动与认知能力恢复等一系列治疗效应(图3)。转录组分析进一步揭示替换细胞重塑了CSF1R相关信号通路和多个神经发育、免疫稳态调控过程,明确了替换治疗的机制基础。
全球首次用于临床,并在人类患者中成功阻断ALSP的病程进展
研究还首次证明,CSF1R缺陷导致的内源小胶质细胞竞争力下降,使得传统骨髓细胞移植(tBMT)可在无辅助药物条件下也实现与Mr BMT相当的小胶质细胞替换效率。ALSP可能是目前已知可通过传统骨髓移植路径实现小胶质细胞替换的唯一神经系统疾病。研究团队进一步在8名确诊ALSP患者中开展基于tBMT的小胶质细胞替换治疗,并完成2年随访。结果显示,患者脑部结构无进展性破坏,PET成像显示小胶质细胞相关葡萄糖代谢显著提升,多个运动和认知功能评分稳定甚至出现改善(图3)。这是全球首次在人类患者中系统验证小胶质细胞替换的临床可行性与长期疗效。该研究也解释了前期被误诊为异染性脑白质营养不良(MLD)的ALSP患者在误诊背景下接受tBMT后病情得到缓解的现象。

图3 基于小胶质细胞替换的细胞治疗策略,通过修正致病基因突变,成功阻断ALSP在小鼠和人类患者中的发生和发展
美国国家医学院院士、华盛顿大学教授Jonathan Kipnis在《Science》上发表了同期专文评述(Perspective)——“ALSP的遗传学基础在十多年前就已被明确,但迄今仍缺乏针对其根本病因的有效治疗方法。本研究的作者通过以野生型骨髓来源的细胞替换携带CSF1R突变的小胶质细胞,成功地在ALSP的小鼠模型和人类患者中阻止了疾病进展,彰显了小胶质细胞替换疗法的治疗前景。”
原文链接:https://doi.org/10.1126/science.adr1015
