学术动态
张从刚/刘翔宇/陈客宏团队《Immunity》发现新型STING激动剂并揭示其作用机制
作者:张从刚 来源自:中国免疫学会 点击数:12340 发布时间:2026-01-16
近日,清华大学药学院张从刚课题组、刘翔宇课题组联合陆军军医大学陆军特色医学中心陈客宏团队,在《Immunity》发表研究论文“A chemical agonist and the Golgi-resident lipid PI4P activate STING by inducing transmembrane helix rearrangement”。该研究系统揭示了一种全新的STING激活机制,并鉴定出新型STING激动剂 GNE-6468,为抗病毒和抗肿瘤免疫治疗提供了新的分子工具与潜在药物先导。
研究团队依托清华大学药学院药物技术中心平台,建立了基于细胞的天然免疫功能筛选体系,对小分子化合物库开展系统筛选,发现 GNE-6468 能在多种细胞体系及人源化小鼠模型中诱导I型干扰素反应,显著激活天然免疫应答。机制分析显示,GNE-6468可显著促进 TBK1–STING–IRF3 信号轴的磷酸化激活,其免疫效应严格依赖STING和TBK1,而不依赖cGAS,提示其为一种直接作用于STING的全新激动剂。
为阐明其分子机制,研究团队利用冷冻电镜技术解析了人源STING–GNE-6468复合物的高分辨率结构。结构结果显示,GNE-6468结合于由STING跨膜螺旋 TM2、TM3 和 TM4 共同构成的跨膜区口袋中,该口袋此前从未被报道。GNE-6468的结合诱导 TM3 螺旋发生显著位移,从而触发STING跨膜区重排并促进其多聚化与激活。同时,研究人员在STING二聚体之间观察到一个脂质分子PI4P。该脂质在结构中发挥类似“分子胶”的作用,与GNE-6468协同稳定STING的激活构象。进一步功能实验表明,靶向 TM2–TM3 loop 的STING抑制剂 H-151,以及抑制PI4P生成的 PI4KB抑制剂,均可在极低浓度下显著抑制GNE-6468诱导的免疫激活效应,从分子和功能层面共同验证了 GNE-6468–PI4P 协同激活STING 的全新机制。
在生物学功能层面,研究发现GNE-6468不仅能够强效诱导I型干扰素反应,还可显著激活非经典自噬,这一特性明显区别于其他已报道的跨膜区STING激动剂(如C53)。在多种人源细胞和样本中,GNE-6468均表现出稳定而强烈的免疫激活能力。进一步的动物实验显示,GNE-6468可通过STING依赖方式产生显著的抗病毒和抗肿瘤免疫效应;同时,其与 PD-1抗体联合用药时,还展现出显著的协同抗肿瘤治疗效果。
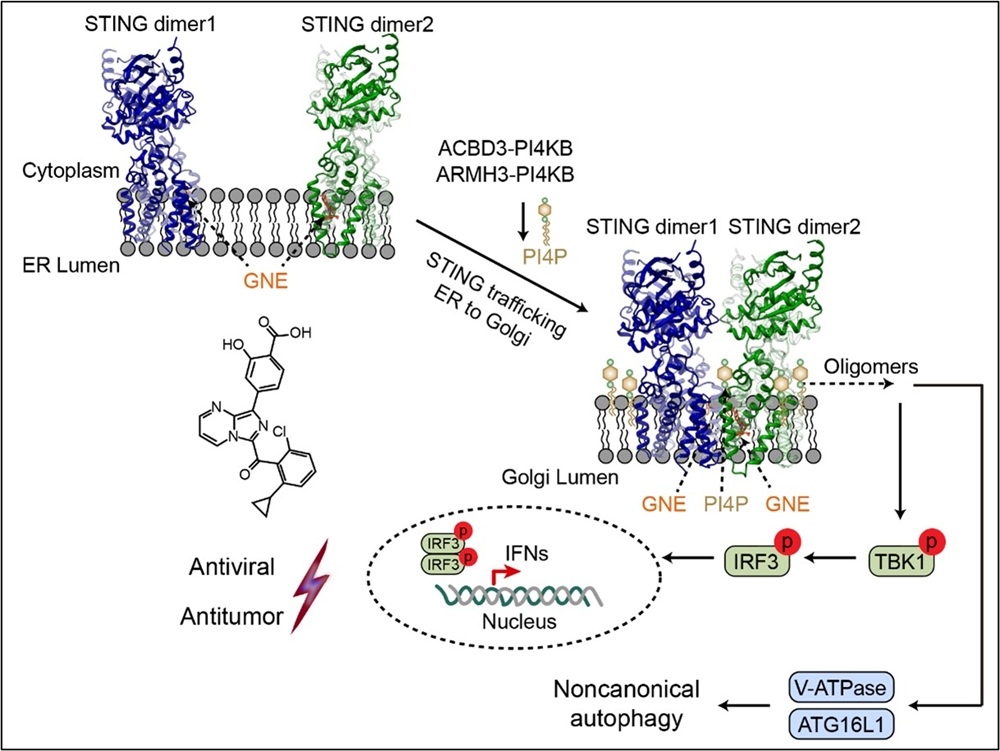
综上,该研究首次揭示了PI4P 参与STING跨膜区构象重排并协同小分子激动剂激活天然免疫信号的分子机制,拓展了人们对脂质免疫调控功能的认识。作为一种靶向全新跨膜区作用位点的高效STING激动剂,GNE-6468在抗感染和抗肿瘤免疫治疗中展现出重要的潜在临床应用价值。
清华大学药学院张从刚、刘翔宇和陆军军医大学陈客宏为该论文通讯作者,韩晶、张书豪、侯燕飞和汪依为该论文第一作者。该研究得到了国家自然科学基金项目、北京市自然科学基金等项目的资助支持。
原文链接:https://www.cell.com/immunity/fulltext/S1074-7613(25)00506-0
研究团队依托清华大学药学院药物技术中心平台,建立了基于细胞的天然免疫功能筛选体系,对小分子化合物库开展系统筛选,发现 GNE-6468 能在多种细胞体系及人源化小鼠模型中诱导I型干扰素反应,显著激活天然免疫应答。机制分析显示,GNE-6468可显著促进 TBK1–STING–IRF3 信号轴的磷酸化激活,其免疫效应严格依赖STING和TBK1,而不依赖cGAS,提示其为一种直接作用于STING的全新激动剂。
为阐明其分子机制,研究团队利用冷冻电镜技术解析了人源STING–GNE-6468复合物的高分辨率结构。结构结果显示,GNE-6468结合于由STING跨膜螺旋 TM2、TM3 和 TM4 共同构成的跨膜区口袋中,该口袋此前从未被报道。GNE-6468的结合诱导 TM3 螺旋发生显著位移,从而触发STING跨膜区重排并促进其多聚化与激活。同时,研究人员在STING二聚体之间观察到一个脂质分子PI4P。该脂质在结构中发挥类似“分子胶”的作用,与GNE-6468协同稳定STING的激活构象。进一步功能实验表明,靶向 TM2–TM3 loop 的STING抑制剂 H-151,以及抑制PI4P生成的 PI4KB抑制剂,均可在极低浓度下显著抑制GNE-6468诱导的免疫激活效应,从分子和功能层面共同验证了 GNE-6468–PI4P 协同激活STING 的全新机制。
在生物学功能层面,研究发现GNE-6468不仅能够强效诱导I型干扰素反应,还可显著激活非经典自噬,这一特性明显区别于其他已报道的跨膜区STING激动剂(如C53)。在多种人源细胞和样本中,GNE-6468均表现出稳定而强烈的免疫激活能力。进一步的动物实验显示,GNE-6468可通过STING依赖方式产生显著的抗病毒和抗肿瘤免疫效应;同时,其与 PD-1抗体联合用药时,还展现出显著的协同抗肿瘤治疗效果。

综上,该研究首次揭示了PI4P 参与STING跨膜区构象重排并协同小分子激动剂激活天然免疫信号的分子机制,拓展了人们对脂质免疫调控功能的认识。作为一种靶向全新跨膜区作用位点的高效STING激动剂,GNE-6468在抗感染和抗肿瘤免疫治疗中展现出重要的潜在临床应用价值。
清华大学药学院张从刚、刘翔宇和陆军军医大学陈客宏为该论文通讯作者,韩晶、张书豪、侯燕飞和汪依为该论文第一作者。该研究得到了国家自然科学基金项目、北京市自然科学基金等项目的资助支持。
原文链接:https://www.cell.com/immunity/fulltext/S1074-7613(25)00506-0
